Un anévrisme est une dilatation dâune artère susceptible de progresser jusquâau moment où il y aura une rupture provoquant une hémorragie massive.
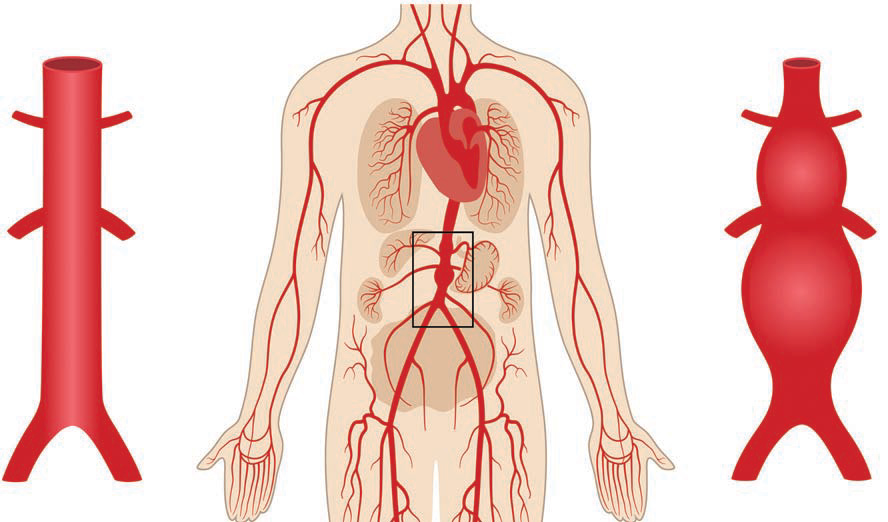
Le vaisseau le plus souvent atteint est l'aorte abdominale distale. On désigne alors cette pathologie par les initiales AAA.
La rupture d'un AAA est associée à une mortalité approchant 90%. Aux États-Unis cet événement serait la troisième cause de mort subite. Au Canada, on rapporte une incidence annuelle de 20,000 nouveaux AAA et de 1250 décès.
90% des AAA sont associés au tabac, plus spécifiquement à la nicotine, et le risque augmente avec l'usage. L'HTA et les dyslipidémies sont des facteurs de risque dont l'impact est beaucoup moindre..
Il existe aussi des facteurs génétiques responsables d'environ 10% des cas.
L'incidence est plus élevée chez les hommes (85%) et augmente avec l'âge, atteignant près de 20% à 80 ans contre moins de 1% avant 60 ans.
Comme c'est une maladie de fumeurs agés, elle coexiste fréquemment avec la vasculopathie athérosclérotique, la MPOC et les néoplasies aéro- digestives.
Par conséquent ces patients ont une espérance de vie inférieure à la moyenne et la majorité va décéder d'une pathologie autre que l'AAA.
Un AAA se définit cliniquement comme une dilatation aortique infra-rénale dont le diamètre maximal est de 30mm ou plus. L'aorte de moins de 30mm n'en est pas pour autant normale. L'ectasie artérielle est un processus progressif et exponentiel, la vitesse de dilatation de l'aorte étant proportionnelle à son diamètre. Il y a consensus qu'un diamètre de 25mm est pathologique (25% vont progresser vers le stade chirurgical) et il est probable que le processus débute à un diamètre inférieur.
Bien que la dilatation aortique soit exponentielle, la progression est initialement très lente. En moyenne il faut 14 ans pour passer de 20 à 30mm, 7 ans entre 30 et 40mm, 4 ans entre 40 et 50mm et 2 ans entre 50 et 60mm.
Comme pour toutes pathologies, la première approche est la prévention. Ici la seule avenue est de cesser de consommer de la nicotine. L'impact sur l'incidence est bien documenté et on a observé une diminution du taux de croissance de 20%. Il n'existe aucun médicament ayant un effet mesurable sur la progression des AAA. Le contrôle de l'HTA et des dyslipidémies a un impact modeste.
La seconde approche est donc curative. Il y a deux façons de traiter un AAA, le pontage par chirurgie ouverte ou le déploiement intravasculaire d'un greffon par accès per-cutané. Chaque technique a des avantages et des inconvénients distincts et leur morbidité n'est pas négligeable. Les chirurgiens vasculaires utilisent des critères spécifiques pour recommander à chaque patient la technique la plus appropriée.
Il n'est pas indiqué d'intervenir précocement, le but est de corriger l'anomalie au moment où le risque de rupture est supérieur à la mortalité opératoire. Le risque annuel de rupture est nul à moins de 40mm et n'est que de 1% entre 40 et 50mm. Ce risque atteint 50% à 80mm. Le standard chirurgical est d'intervenir quand l'anévrisme atteint un diamètre de 55mm.
L'AAA est asymptomatique jusqu'à sa rupture et sa détection par l'examen physique est peu fiable. Seule l'imagerie médicale est à la fois sensible et spécifique. En raison de sa localisation l'AAA peut être facilement évalué par l'échographie. La tomodensitométrie et l'IRM sont également excellents mais leur utilisation chez un patient asymptomatique est un usage inapproprié de ressources limitées.
La question du dépistage est pertinente mais elle n'a pas encore été résolue de façon définitive. Depuis 30 ans il y a eu de nombreux projets pilotes à travers le monde. Aujourd'hui, seuls le Royaume-Uni et la Suède ont un dépistage systématique qui, dans chaque cas, invite tous les hommes entre 65 et 75 ans à une évaluation échographique de leur aorte et qui s'assure du suivi et du traitement des cas positifs. Les femmes sont exclues en raison d'une incidence trop faible et de la moindre efficacité des interventions curatives chez elles. Les programmes britanniques et suédois ont été mis en place entre 2006 et 2015 mais leurs résultats sont ambigus. Ils seraient associés à une réduction de 43% du nombre de décès par rupture. Par contre, ils ont également permis de constater que la prévalence de la pathologie a diminué de moitié depuis les projets pilotes.
Une analyse des statistiques a conclu que la réduction du tabagisme depuis 30 ans a un impact beaucoup plus significatif sur la mortalité par AAA que le dépistage.
Au Québec, en 2010, l'Agence d'évaluation des technologies et des modes d'intervention en santé a publié une évaluation sur la pertinence d'un programme de dépistage. Copier le modèle européen permettrait d'éviter 100 décès par année. Or ce résultat présume d'une prévalence de 5% dans le groupe cible alors que les européens, qui avaient au départ la même prémisse, constatent aujourd'hui une prévalence de 2%. La réduction du tabagisme au Québec depuis 30 ans se comparant à celle des deux pays mentionnés laisse présumer que l'impact d'un dépistage serait modeste.
Aucune recommandation n'avait alors été faite et le Québec, tout comme le reste du Canada, n'a pas de programme de dépistage.
Il n'est pas pour autant contre-indiqué de procéder à une évaluation préventive chez un groupe ciblé d'individus asymptomatiques mais à risque en tenant compte de l'accessibilité des ressources.
Cette conduite doit donc être déterminée en fonction des conditions locales. Comme il n'y a pas de normes nationales chaque communauté médicale doit déterminer, conjointement avec ses spécialistes en imagerie et en chirurgie vasculaire, sa propre liste de critères quant aux patients à dépister, la gestion des résultats d'échographie, les intervalles de suivi et le moment où le patient doit être référé au chirurgien.
Cet exercice a été fait dans ma région, l'Abitibi- Témiscamingue, il y a moins d'un an.
Nos critères d'inclusion sont:
Notre critère d'exclusion:
Nos critères d'un examen normal sont:
Notre guide de suivi échographique est:
Peu importe les circonstances , il doit y avoir cessation de la consommation de nicotine sous toutes ses formes.