« Les bénéfices attendus du théranostic sont une prescription plus sûre (thérapie ciblée, médecine de précision) grâce à l’identification de patients répondeurs à moindre risque de toxicité, l’identification et la réduction des effets iatrogènes, la prise en charge plus précoce de pathologies, l’optimisation des coûts de santé (pharmacoéconomie).»

En préalable, il convient de préciser la signification du terme « théranostic » qui en tant que substantif est du genre masculin comme « diagnostic » et « pronostic » dans les textes réglementaires mais souvent du genre féminin dans la langue parlée influencée par « thérapie » et par l’orthographe de l’adjectif.
Le Dictionnaire de l’Académie Nationale de Pharmacie française le définit en 2018 comme « un néologisme issu de la contraction des termes " thérapie " et " diagnostic " [correspondant à une] pratique médicale basée sur l'utilisation d'un test diagnostique permettant d'orienter la thérapeutique d'un patient. Le test diagnostique, appelé « test compagnon » (d’utilisation du traitement) consiste en l'identification d'un biomarqueur dont le statut (présence, absence, surexpression, forme mutée...) sera un témoin d'un processus biologique et son évolution un indicateur prédictif de la réponse au traitement. Les bénéfices attendus du théranostic sont une prescription plus sûre (thérapie ciblée, médecine de précision) grâce à l’identification de patients répondeurs à moindre risque de toxicité, l’identification et la réduction des effets iatrogènes, la prise en charge plus précoce de pathologies, l’optimisation des coûts de santé (pharmacoéconomie). De plus en plus de médicaments ne peuvent être prescrits qu’après avoir obtenu une réponse positive du test théranostique compagnon, car le processus d’autorisation de mise sur le marché est conjoint (couplage [de l’autorisation de mise sur le marché] (AMM) du médicament et du marquage CE du théranostic) ».
Selon cette définition, l’imagerie diagnostique de médecine nucléaire a toujours eu une dimension théranostique puisque les images qu’elle procure ont pour but de mettre en évidence la fonction, le métabolisme ou des particularités biologiques des organes ou tissus, avec souvent pour conséquence directe d’orienter la prise en charge médicale ou chirurgicale des patients. Parmi les nombreux exemples de ce théranostic pluri-décennal en médecine nucléaire, citons : la caractérisation d’un nodule thyroïdien comme autonome conduisant à l’ablation, l’objectivation d’une ischémie myocardique, l’asymétrie de fonction entre les deux reins prise en charge par chirurgie ou par traitement médical, la découverte de l’extension oligométastatique d’un cancer en tomographie par émission de positons (TEP) guidant la radiothérapie ou la chimiothérapie, l’évaluation de la réponse ou de la résistance au traitement d’un lymphome en TEP avec le sucre analogue radioactif du glucose FDG ...
En revanche, les exemples pratiques d’application théranostique que donne ensuite l’Académie de Pharmacie française et ceux que prennent en compte les agences réglementaires française et européenne ne font pas actuellement la part belle à la médecine nucléaire. Le « test compagnon » sur lequel porte actuellement l’effort de rationalisation réglementaire de l’agence européenne du médicament (EMA) est un test diagnostique in vitro, par exemple la détection d’un marqueur en immunohistochimie, d’une mutation génique, sur biopsie ou sur cellules circulantes. Il s’agit donc d’un dispositif médical devant disposer du marquage CE.
Grâce à l’imagerie nucléaire (TEP principalement), les compagnons diagnostiques radioactifs mettent en évidence et localisent, in situ et de façon non invasive, les tissus cibles anormaux surexprimant tel récepteur ou tel antigène à la suite d’une mutation. Ce ne sont pas des dispositifs médicaux mais des médicaments de diagnostic. Par rapport aux tests pratiqués in vitro sur des spécimens prélevés in vivo de façon plus invasive, ils présentent l’avantage ne pas se borner à caractériser une seule lésion biopsiable ou un nombre restreint de lésions. Ils caractérisent la présence ou l’absence de l’anomalie caractéristique au sein de toutes les lésions macroscopiques, au niveau du corps entier, en un seul examen. Il est important que l’imagerie TEP permette cette caractérisation pour chaque lésion macroscopique, car les métastases peuvent présenter, par rapport à la tumeur primitive, une expression des récepteurs ou des antigènes anormaux ou des mutations qui est différente et variable entre elles. La prise en compte de cette possible hétérogénéité est un apport dans la prise en charge théranostique.
De plus, le caractère non invasif de la TEP permet de répéter l’examen avec le compagnon diagnostic durant le suivi. Il est possible que l’action de l’agent thérapeutique aboutisse à favoriser les cellules ou les lésions tumorales qui ne présentent pas ou plus l’anomalie ciblée. Vérifier la persistance et l’étendue des lésions qui peuvent répondre à l’agent thérapeutique permet d’adapter si nécessaire la thérapie en cours, sans multiplier les biopsies, évitant de poursuivre un protocole thérapeutique inefficace et coûteux. C’est la contribution du théranostic nucléaire à la « médecine personnalisée de précision ».
Comme conséquence de son administration au patient, le compagnon diagnostique pour l’imagerie nucléaire doit disposer d’une AMM incluant l’approche théranostique, tout comme le médicament thérapeutique. Ceci implique l’évaluation approfondie de son bénéfice pour le patient, le risque se limitant à une faible radioexposition sans conséquence connue. Mais cette phase d’évaluation par les agences du médicament aboutit souvent à un allongement des délais de mise à disposition par rapport à l’obtention du marquage CE, et son coût peut être difficile à supporter par des petites firmes développant un théranostic innovant.
Lors d’une réunion avec l’EMA en septembre 2021, l’organisation Nuclear Medicine Europe (NMEU) a cité les médicaments nucléaires théranostiques, parmi « les médicaments nucléaires pour lesquels un cadre réglementaire plus clair serait bénéfique, compte tenu de leur potentiel élevé en médecine de précision pour le cancer ou dans les applications de neuroimagerie. »
Le tableau ci dessous rapporte la pratique actuelle de la médecine nucléaire dans l’application théranostique en France. Nous nous sommes volontairement limités aux applications où il existe une proximité de structure chimique et de mode de liaison aux cibles à traiter entre les deux médicaments diagnostique et thérapeutique et où l’un des deux au moins est radioactif.
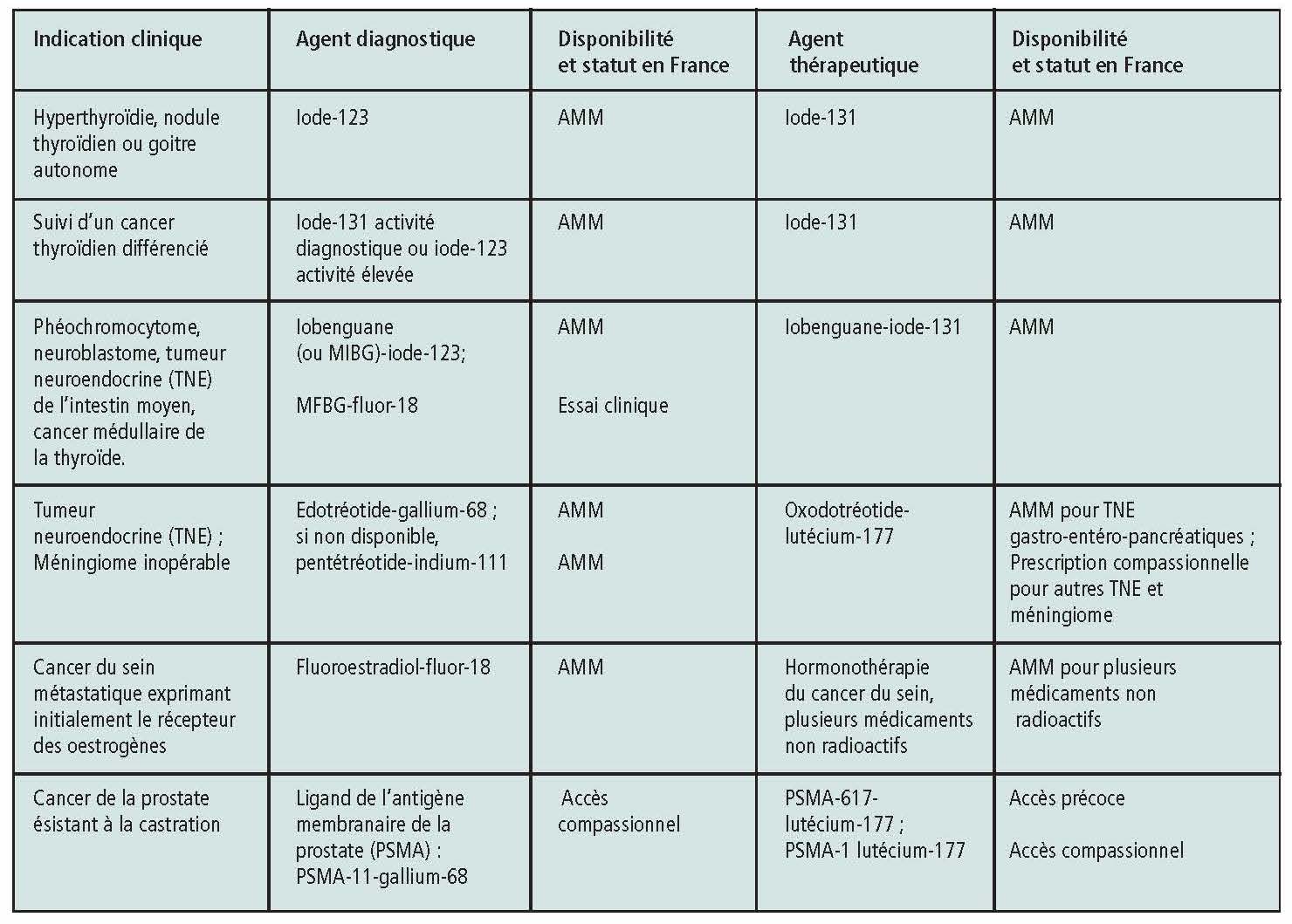
De nombreux autres couples théranostiques, compagnon diagnostique et médicament de radiothérapie interne vectorisée, sont actuellement décrits, certains au stade de l’évaluation préclinique chez l’animal, d’autres déjà en cours d’essai clinique. Il est difficile de prévoir lesquels obtiendront finalement une AMM dans un avenir proche. Beaucoup de candidats sont positionnés avec des indications potentielles multiples en cancérologie, le cancer de la prostate, le cancer du sein, les gliomes et/ou les hémopathies malignes …, dont des médicaments de la famille de la bombésine, des ligands des récepteurs des chemokines ou des intégrines, des inhibiteurs radiomarqués de la protéine d’activation des fibroblastes (FAPI) ciblant le stroma de divers cancers. Dans le cas de la radioimmunothérapie, l’agent thérapeutique est un anticorps radiomarqué. L’étape de contrôle du ciblage par test compagnon, possible avec le même anticorps marqué par un agent radioactif pour l’imagerie TEP (cuivre-64 ou zirconium-89), peut poser problème, car elle risque d’entrainer chez le patient l’apparition d’anticorps dirigés contre l’agent thérapeutique potentiel, qui risquait alors d’être inactivé. Cependant certains essais de théranostic sont en cours, par exemple avec le girentuximab marqué au zirconium-89 puis au lutécium-177, ciblant une enzyme, l’anhydrase carbonique IX, surexprimée dans certains cancers du rein. On voit même l’évolution inverse se produire : le daratumumab-cuivre-64 pour la TEP est en essai clinique comme agent diagnostique bien après que le daratumumab a obtenu une AMM dans l’UE pour le traitement du myélome.
En conclusion, selon l’acception large de ce terme relativement récent, la médecine nucléaire fait du théranostic depuis ses origines. Une acception, plus restreinte mais plus commune, du terme théranostic correspond à l’existence d’un test compagnon permettant la sélection des patients pour maximiser les chances de réponse favorable à un médicament thérapeutique qui lui est apparenté par la structure chimique ou étroitement lié par le mécanisme d’action. Dans cette approche, la médecine nucléaire a de gros atouts grâce à la TEP, tout d’abord en préclinique, pour vérifier la sensibilité et la spécificité du ciblage tumoral dans des modèles animaux, puis chez l’Homme. Le foisonnement de projets de théranostic nucléaire auquel on assiste actuellement en témoigne.